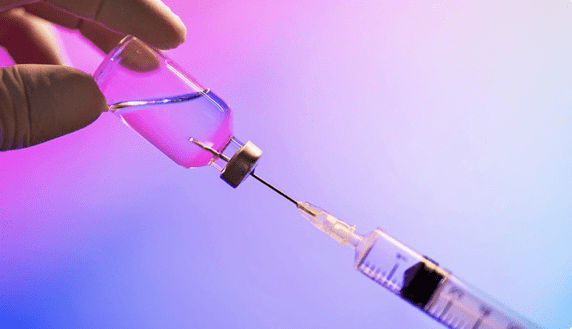
La FDA autorizó el uso de Yeztugo, de Gilead Sciences, convirtiéndose en el primer tratamiento de larga duración contra el VIH.
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó el uso de Yeztugo (lenacapavir), una inyección desarrollada por la farmacéutica Gilead Sciences, que previene el contagio del VIH con solo dos dosis al año. Se trata del primer tratamiento profiláctico de acción prolongada que ha demostrado una efectividad superior al 99 % en ensayos clínicos, abriendo una nueva era en la prevención del virus.
El medicamento fue evaluado en estudios realizados en África y América, especialmente entre mujeres jóvenes, hombres homosexuales y personas transgénero, obteniendo resultados sin precedentes: 100 % de eficacia en mujeres y 99,9 % en otros grupos vulnerables. Su mecanismo actúa como barrera preventiva frente a una posible exposición al virus, lo que podría transformar las estrategias globales de salud pública frente al VIH.
Entre sus ventajas se destaca que no requiere una toma diaria, como ocurre con otros tratamientos de PrEP, lo que mejora la adherencia y reduce el estigma. Sin embargo, su alto costo en Estados Unidos —más de 28.000 dólares anuales— ha despertado preocupación en organizaciones como ONUSIDA, que exigen mecanismos de acceso justo y precios asequibles en países de ingresos medios y bajos.
Gilead anunció convenios con fabricantes de medicamentos genéricos para facilitar su distribución en más de 120 países en desarrollo, beneficiando a dos millones de personas en una primera etapa. Expertos en salud pública consideran que esta aprobación representa un paso histórico en la lucha contra el VIH, pero advierten que su éxito dependerá de una implementación equitativa y global.